식약당국의 품목허가 심사 인력이 해외 선진국보다 절대적으로 부족해 기업들의 신약 출시와 글로벌 진출을 제대로 지원하기 위해서는 예산 확보와 인력 확충이 시급하다는 목소리가 높다.
제약·바이오 업계에 따르면, 신약을 개발해도 허가심사나 품질을 평가할 인력이 부족해 적시에 승인이 이뤄지지 않는 경우가 많아 기업들이 신약을 출시하는데 어려움이 큰 상황이다. 심사 인력이 부족하다보니 민원 신청 즉시 심사가 진행되지 못하고 처리 기간이 임박해 심사와 보완이 발생해 실제 처리 기간은 훨씬 많이 소요되는 악순환이 계속되는 실정이다.
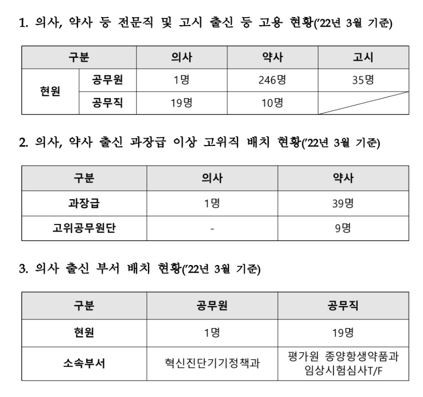
식품의약품안전처가 최근 전문지기자단에 공개한 '의사·약사 등 전문인력 고용 현황'을 보면, 2022년 3월 기준 전문직 및 고시 출신 공무원은 의사 1명, 약사 246명, 한약사, 33명, 고시 출신 35명이다. 전문인력 중 약사가 가장 많은 비율(약 78%)을 차지했다.

약사의 경우 국·청 단위로 본부 직속 등에 64명, 의약품안전국에 51명, 바이오생약국에 25명, 식품의약품안전평가원에 78명, 6개 지방청에 28명이 배치됐다.
한약사는 본부 직속 등 3명, 의약품안전국 6명, 바이오생약국 4명, 식품의약품안전평가원 3명, 6개 지방청 17명 배치됐다. 약사는 식품의약품안전평가원에, 한약사는 6개 지방청에 가장 많은 인원이 배치돼 있다.
2022년 3월 기준 식약처의 과장 이상 보직 인원은 132명이다. 이중 의사는 1명, 약사는 35명이다. 과장급(4급 이상) 이상 보직과 과장(부서장) 보직은 다른 개념으로 과장급 이상을 기준으로 봤을 때 약사는 39명이다.
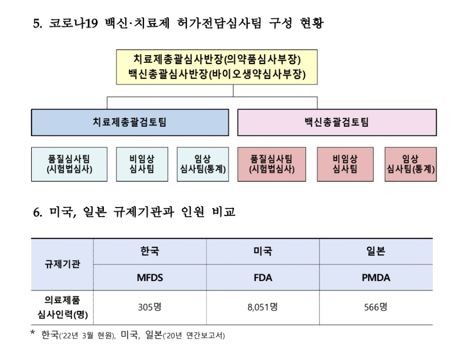
식약처의 허가심사 인력 부족 문제는 해마다 제기되던 사안으로 식약처 국정감사에서도 매번 지적된다. 제약·바이오업계는 식약처의 의약품 허가심사나 품질평가 전문성이 질적·양적 측면에서 매우 부족하다고 평가해왔다.
한국제약바이오협회 자료를 보면, 국산 신약 개발을 위한 투자와 연구 노력이 이어지고 있지만, 허가가 취소되거나 중도 탈락하는 경우가 많아 글로벌 바이오의약품 시장 점유율은 1.3%에 그친다. 미국 40.5%, 유럽 13.2%, 중국 11.8%에 못 미치는 수치다.
이같은 원인으로 규제과학 인력과 인프라가 절대적으로 부족하다는 점이 꼽힌다. 해외 규제 당국의 의료제품 심사인력은 한국 대비 미국이 35.3배, 유럽은 17.5배, 캐나다 5.1배, 일본 2.5배 등이다.
업계 관계자들은 새정부에서는 식약처의 허가 심사 인력을 대폭 늘리고 각 신약 개발 전 주기를 총괄할 체제가 반드시 만들어져야 한다고 강조하고 있다.
식약처 관계자는 "예산을 업체들에 나눠주는 것보다 의사 인력 1명을 뽑는데 쓴다면 경제적 파급효과와 환자 혜택이 더 클 것"이라면서 "정규직 인원을 늘려 안정적인 업무가 이뤄지는 게 최선이지만 인력 확충의 경우 기획재정부와 협의를 해야 하다보니 쉽지만은 않은 상황"이라고 전했다.
한편 식약처는 매년 민간경력채용과 자체채용을 통해 의사, 약사 등 전문인력을 충원 중이다. 현재 코로나19 백신과 치료제 제품화 지원 인력을 충원하기 위해 전문임기제 공무원(13명)의 경력 경쟁채용을 진행 중이다.
이원식 기자의 전체기사 보기
Copyright @보건신문 All rights reserved.